Công bố các cơ sở kinh doanh có dược liệu, vị thuốc cổ truyền vi phạm chất lượng
 |
Đây là đợt công bố thứ 8 của Cục Quản lý y, dược cổ truyền (tổng hợp các trường hợp vi phạm từ ngày 01/01/2021 đến ngày 30/5/2021).
Trong danh sách đợt này có Công ty TNHH dược liệu Vinh Thoa (địa chỉ tại 127 Lê Thánh Tông, Buôn Ma Thuột, Đắk Lắk); Phòng chẩn trị YHCT Phùng Nồng (địa chỉ tại 356 Hùng Vương, Đà Nẵng); Phòng chẩn trị YHCT Nhơn Hoà Đường (địa chỉ tại 157 Nguyễn Thuỵ, Quảng Ngãi);
Phòng chẩn trị YHCT Minh Tâm Đường (địa chỉ tại số 5 Trường Sơn, Pleiku, Gia Lai); Cơ sở Đại Nguyên Đường (địa chỉ tại số 05 Phạm Thái, ấp thị II, TT. Chợ Mới, Chợ Mới, tỉnh An Giang); Cơ sở kinh doanh thuốc YHCT Đức Phú Đường (địa chỉ tại 331/4 Hùng Vương, Đà Nẵng).
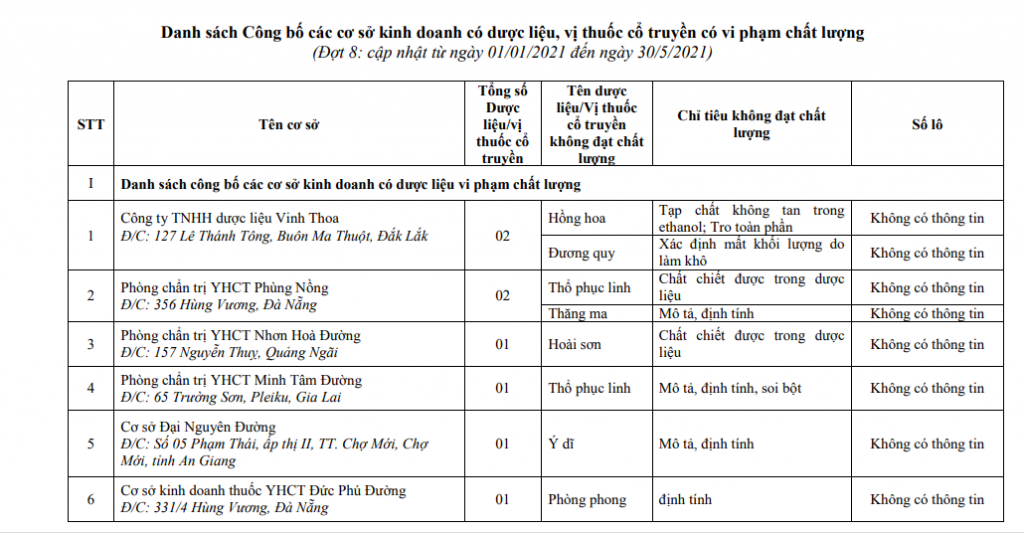 |
| Danh sách các cơ sở kinh doanh có dược liệu, vị thuốc cổ truyền vi phạm chất lượng. |
Quản lý chất lượng dược liệu, vị thuốc cổ truyền trong kinh doanh
Liên quan tới vấn đề quản lý chất lượng dược liệu, vị thuốc cổ truyền, Bộ Y tế đang dự thảo Thông tư quy định về chất lượng dược liệu, thuốc cổ truyền. Bộ đề xuất quy định quản lý chất lượng dược liệu, vị thuốc cổ truyền, thuốc cổ truyền trong quá trình kinh doanh, lưu hành, sử dụng.
Cụ thể, Bộ Y tế đề xuất yêu cầu quản lý chất lượng dược liệu, vị thuốc cổ truyền, thuốc cổ truyền trong quá trình kinh doanh như sau: Áp dụng các nguyên tắc, tiêu chuẩn Thực hành tốt trong suốt quá trình kinh doanh, phù hợp với phạm vi kinh doanh của cơ sở. Đối với cơ sở chuyên bán lẻ dược liệu, vị thuốc cổ truyền, thuốc cổ truyền thì phải áp dụng các điều kiện bán lẻ dược liệu, vị thuốc cổ truyền, thuốc cổ truyền trong suốt quá trình kinh doanh theo quy định hiện hành.
Dược liệu, nguyên liệu sản xuất thuốc cổ truyền, bao bì tiếp xúc trực tiếp với thuốc cổ truyền trước khi đưa vào sản xuất thuốc cổ truyền phải được cơ sở sản xuất tiến hành kiểm nghiệm và đạt tiêu chuẩn chất lượng. Dược liệu, vị thuốc cổ truyền, thuốc cổ truyền trước khi xuất xưởng phải được cơ sở sản xuất tiến hành kiểm nghiệm và đạt tiêu chuẩn chất lượng.
Người đứng đầu và người phụ trách chuyên môn của cơ sở kinh doanh; người phụ trách về bảo đảm chất lượng của cơ sở sản xuất phải chịu trách nhiệm về công tác quản lý chất lượng và kiểm tra chất lượng dược liệu, thuốc cổ truyền tại cơ sở.
Dự thảo nêu rõ, cơ sở kinh doanh dược liệu, vị thuốc cổ truyền, thuốc cổ truyền có trách nhiệm tổ chức và thực hiện công tác kiểm tra, kiểm soát chất lượng dược liệu, nguyên liệu phục vụ sản xuất thuốc cổ truyền, thuốc cổ truyền tại cơ sở. Cơ sở kinh doanh dược liệu, vị thuốc cổ truyền, thuốc cổ truyền phải tổ chức công tác kiểm tra, kiểm nghiệm để xác định, đánh giá được chất lượng của dược liệu, thuốc cổ truyền, nguyên liệu sử dụng sản xuất thuốc cổ truyền trong suốt quá trình sản xuất, xuất xưởng, lưu hành.
Cơ sở kinh doanh dược liệu, vị thuốc cổ truyền, thuốc cổ truyền phải lưu giữ các hồ sơ, tài liệu, thông tin liên quan đến mỗi lần mua bán, nhập khẩu, xuất xưởng, phân phối, lưu hành dược liệu, vị thuốc cổ truyền, thuốc cổ truyền nhằm bảo đảm truy xuất được nguồn gốc, xuất xứ, kiểm soát được toàn bộ đường đi, điều kiện bảo quản của dược liệu, vị thuốc cổ truyền, thuốc cổ truyền và nguyên liệu sử dụng sản xuất thuốc cổ truyền.
Cơ sở kinh doanh dược liệu, vị thuốc cổ truyền, thuốc cổ truyền có trách nhiệm chi trả chi phí kiểm nghiệm, cung cấp dược liệu đối chiếu, chất chuẩn, chất đối chiếu cho cơ quan kiểm nghiệm trong trường hợp cơ quan kiểm nghiệm chưa nghiên cứu thiết lập được đối với mẫu dược liệu, vị thuốc cổ truyền, thuốc cổ truyền gửi kiểm nghiệm của chính cơ sở.
Cơ sở có trách nhiệm thực hiện các quy định khác của phát luật về dược nhằm bảo đảm, duy trì chất lượng dược liệu, thuốc cổ truyền trong suốt quá trình kinh doanh, lưu hành và sử dụng.
 |
| Dự thảo Thông tư quy định về chất lượng dược liệu, thuốc cổ truyền (ảnh minh họa) |
Quản lý chất lượng tại cơ sở khám bệnh, chữa bệnh
Theo dự thảo, dược liệu, vị thuốc cổ truyền, thuốc cổ truyền sử dụng tại cơ sở khám bệnh, chữa bệnh phải có phiếu kiểm nghiệm đạt tiêu chuẩn chất lượng theo tiêu chuẩn dược điển hoặc tiêu chuẩn cơ sở theo hồ sơ đăng ký lưu hành vị thuốc cổ truyền, thuốc cổ truyền và hồ sơ công bố tiêu chuẩn chất lượng dược liệu.
Dược liệu, vị thuốc cổ truyền, thuốc cổ truyền phải được kiểm tra, kiểm nhập thông qua Hội đồng kiểm nhập của bệnh viện quy định tại Thông tư số 22/2011/TT-BYT ngày 10/6/2011 của Bộ trưởng Bộ Y tế quy định tổ chức và hoạt động của Khoa Dược bệnh viện hoặc bộ phận kiểm nhập của cơ sở khám bệnh, chữa bệnh khác.
Đối với thuốc cổ truyền do cơ sở khám bệnh, chữa bệnh chế biến, bào chế theo quy định tại Điều 70 Luật dược: Cơ sở khám bệnh, chữa bệnh phải thực hiện kiểm nghiệm chất lượng thuốc cổ truyền tại cơ sở kiểm nghiệm thuốc, nguyên liệu làm thuốc của Nhà nước hoặc cơ sở kinh doanh dịch vụ kiểm nghiệm thuốc, nguyên liệu làm thuốc đã được cấp Giấy chứng nhận đủ điều kiện kinh doanh thuốc. Trường hợp, cơ sở khám bệnh, chữa bệnh có Phòng kiểm nghiệm thuốc đạt Thực hành tốt Phòng thí nghiệm thuốc thì được thực hiện kiểm nghiệm chất lượng thuốc tại cơ sở.
Đối với vị thuốc cổ truyền do cơ sở khám bệnh, chữa bệnh sản xuất mà có hoạt động bán cho cơ sở khám bệnh, chữa bệnh khác theo quy định tại Khoản 2 Điều 70 Luật dược thì phải thực hiện kiểm nghiệm chất lượng vị thuốc cổ truyền tại cơ sở kiểm nghiệm thuốc, nguyên liệu làm thuốc của Nhà nước hoặc cơ sở kinh doanh dịch vụ kiểm nghiệm thuốc, nguyên liệu làm thuốc đã được cấp Giấy chứng nhận đủ điều kiện kinh doanh thuốc. Trường hợp, cơ sở khám bệnh, chữa bệnh có Phòng kiểm nghiệm thuốc đạt Thực hành tốt Phòng thí nghiệm thuốc thì được thực hiện kiểm nghiệm chất lượng thuốc tại cơ sở.
Người đứng đầu cơ sở khám bệnh, chữa bệnh có trách nhiệm tổ chức kiểm tra định kỳ ít nhất 3 tháng một lần và kiểm tra đột xuất khi cần thiết về chất lượng dược liệu, thuốc cổ truyền trong cơ sở khám bệnh, chữa bệnh. Kết quả kiểm tra phải được lập thành biên bản.
Trường hợp phát hiện có yếu tố nguy cơ ảnh hưởng đến chất lượng dược liệu, thuốc cổ truyền, cơ sở khám bệnh, chữa bệnh phải gửi mẫu đến cơ sở kiểm nghiệm thuốc, nguyên liệu làm thuốc của Nhà nước hoặc cơ sở kinh doanh dịch vụ kiểm nghiệm thuốc, nguyên liệu làm thuốc đã được cấp Giấy chứng nhận đủ điều kiện kinh doanh thuốc để kiểm nghiệm, kiểm tra chất lượng.
Có thể bạn quan tâm
Cùng chuyên mục
Tin khác

Siết chặt giám sát, cảnh báo sớm để bảo đảm an toàn thực phẩm nông, lâm, thủy sản

Siết an toàn bếp ăn học đường sau vụ “thịt ôi, trứng hỏng” tại Trường Tiểu học Cự Khê

Longevity Medical Center và Fujifilm: Kết nối công nghệ AI với triết lý chăm sóc sức khỏe trường thọ

COQ10-STELLA – Giải pháp hỗ trợ chống oxy hoá, góp phần duy trì sức khỏe tim mạch

Herbalife Việt Nam đồng hành “Ngày Dinh dưỡng cộng đồng” lần 5, tư vấn cho hơn 1.350 người

WHO báo động: Thanh thiếu niên hút thuốc lá điện tử nhiều gấp 9 lần người lớn
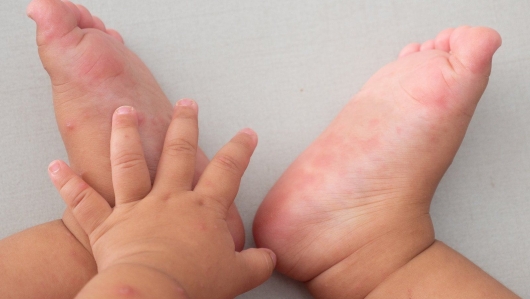
Bệnh tay chân miệng bùng phát mạnh, Bộ Y tế ra công văn khẩn

Thu hồi toàn quốc kem thảo dược và dung dịch vệ sinh vi phạm

Bão số 11 Matmo có hai kịch bản ảnh hưởng trực tiếp tới miền Bắc




















